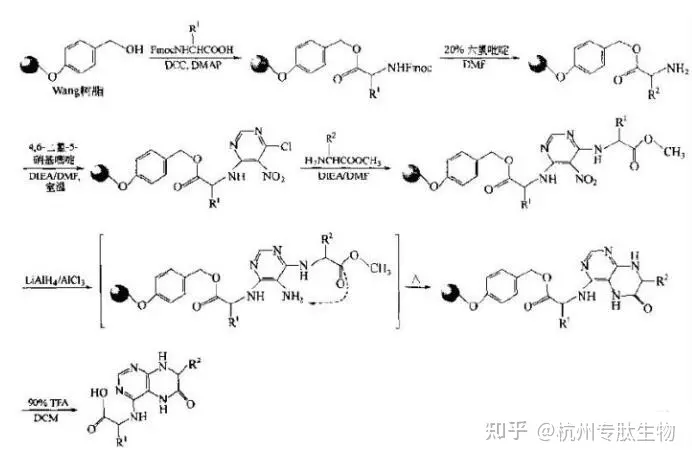
3-去氧-D-甘露-辛酮糖酸(Kdo)是一种单糖,这是细菌表面多糖的重要组成部分,广泛存在于细菌的脂多糖及荚膜多糖中。其对维持细菌细胞壁以及外膜的完整性具有重要作用。如果能实现 Kdo 糖苷的高效率、高选择性合成,将为抗菌疫苗及新型抗生素的开发带来更多新的选择。然而,目前 Kdo 糖基化面临着难以控制选择性、反应活性低等诸多难题和挑战。不久前,北京大学药学院的研究人员报道了一种高效简洁的糖基化方法,这是一种合成 α-Kdo (α-3-Deoxy-d-manno-oct-2-ulosonic Acid)糖苷的间接方法,即通过 3 位硫醚取代 Kdo 糖基供体高效合成一系列 α-Kdo 糖苷,产率最高达 98%。然后,通过分步或一锅法合成了多种天然低聚糖,包括 Kdo 五糖。这项研究已经发表在了 Angewandte Chemie International Edition 上。
3-去氧-D-甘露-辛酮糖酸(Kdo)是一种单糖,这是细菌表面多糖的重要组成部分,广泛存在于细菌的脂多糖及荚膜多糖中。其对维持细菌细胞壁以及外膜的完整性具有重要作用。如果能实现 Kdo 糖苷的高效率、高选择性合成,将为抗菌疫苗及新型抗生素的开发带来更多新的选择。然而,目前 Kdo 糖基化面临着难以控制选择性、反应活性低等诸多难题和挑战。不久前,北京大学药学院的研究人员报道了一种高效简洁的糖基化方法,这是一种合成 α-Kdo (α-3-Deoxy-d-manno-oct-2-ulosonic Acid)糖苷的间接方法,即通过 3 位硫醚取代 Kdo 糖基供体高效合成一系列 α-Kdo 糖苷,产率最高达 98%。然后,通过分步或一锅法合成了多种天然低聚糖,包括 Kdo 五糖。这项研究已经发表在了 Angewandte Chemie International Edition 上。 (来源:Angewandte Chemie International Edition)本研究的通讯作者是北京大学药学院化学生物学系主任、教授李中军和助理研究员李忠堂。李中军的重点研究方向是探索寡糖合成方法学及快速组装策略、糖为手性源的天然产物和合成与活性、 基于糖的化学生物学研究以及创新药物研发。Kdo 糖基化是合成多种 α-Kdo 糖苷的重要方法,然而这是最具挑战性的糖基化反应之一。也因此,领域内一直在探索开发出高效且具有立体选择性的糖基化方法。现阶段,领域内已经开发出了多种方法,包括直接法和间接法。前者需要选择合适的保护基,且糖基化过程会产生 2,3-烯(2,3-ene)副产物;间接法通常需要添加一个或多个步骤构建具有完全立体调节性的目标糖苷,与直接方法相比,这种方法极大简化了保护基的选择,提高了效率和立体选择性。不过,间接法存在增加了反应步骤,且不易选择合适的辅助基团等问题。在这项研究中,该团队开发出了一种更高效、便捷实现 Kdo 糖基化的间接方法。他们通过轴向键在 Kdo 的 C3 位置上引入对甲苯硫基(p-tolylthio group),基于经修饰的 Kdo 亚磷酸酯供体合成了多种 α-Kdo 糖苷和几种极具挑战性的 Kdo 寡糖。值得一提的是,这一过程中并没有形成 2,3-烯副产物,对甲苯硫基也可以通过自由基还原轻松清除。
(来源:Angewandte Chemie International Edition)本研究的通讯作者是北京大学药学院化学生物学系主任、教授李中军和助理研究员李忠堂。李中军的重点研究方向是探索寡糖合成方法学及快速组装策略、糖为手性源的天然产物和合成与活性、 基于糖的化学生物学研究以及创新药物研发。Kdo 糖基化是合成多种 α-Kdo 糖苷的重要方法,然而这是最具挑战性的糖基化反应之一。也因此,领域内一直在探索开发出高效且具有立体选择性的糖基化方法。现阶段,领域内已经开发出了多种方法,包括直接法和间接法。前者需要选择合适的保护基,且糖基化过程会产生 2,3-烯(2,3-ene)副产物;间接法通常需要添加一个或多个步骤构建具有完全立体调节性的目标糖苷,与直接方法相比,这种方法极大简化了保护基的选择,提高了效率和立体选择性。不过,间接法存在增加了反应步骤,且不易选择合适的辅助基团等问题。在这项研究中,该团队开发出了一种更高效、便捷实现 Kdo 糖基化的间接方法。他们通过轴向键在 Kdo 的 C3 位置上引入对甲苯硫基(p-tolylthio group),基于经修饰的 Kdo 亚磷酸酯供体合成了多种 α-Kdo 糖苷和几种极具挑战性的 Kdo 寡糖。值得一提的是,这一过程中并没有形成 2,3-烯副产物,对甲苯硫基也可以通过自由基还原轻松清除。 (来源:上述论文)确定亚磷酸酯之后,该团队进行了底物范围研究,在糖基亚磷酸酯供体活化条件下,经修饰的 Kdo 亚磷酸酯糖基供体 1 可以在 5 分钟内完全活化,并产生了 Kdo 糖苷 3a,其产率 为 91%,且未形成 2,3-烯副产物。接下来,经修饰的 α-Kdo 亚磷酸酯供体 1与各种受体 2a- 2r 进行糖基化反应,产生 Kdo 糖苷 3a-3r 的产率约为 79%-97%之间。随后,该团队筛选了⼀系列自由基反应去除对甲苯硫基,选定条件下,大部分对甲苯硫基被有效去除,且生产 α-Kdo 糖苷产物 4a‒4o 的产率在 79%‒96%。然后,将供体 1 与一级和次级糖基受体 5a-5l 偶联产生 α-Kdo 二糖 6a–6l,产率约在 85%–98% 区间。为了证明亚磷酸酯供体 1 和硫代糖苷的正交性,研究团队合成了硫代葡萄糖苷受体 5j‒5l 并分别与供体 1 偶联,结果显示所合成的 α-Kdo 的二糖 6j、6k 以及 6l,产率分别是 90%、90% 和 85%。为了验证上述方法在生成 Kdo 天然低聚糖中的实用性,研究团队尝试合成 Kdo-α-(2→6)-GlcN-β-(1→6)-GlcN 三糖。在试验中,他们以供体 12 和 6-OH 受体在 5 天内合成葡萄糖胺二糖 13,优化条件后,最终得到三糖 15 的产量率为 93%。去除对甲苯硫基后,三糖 16 的产率为 82%。通过一系列试验,研究人员证明了亚磷酸酯供体和硫代糖苷供体的正交性,这为构建 Kdo 复合寡糖提供了新的选择。后续,研究团队还合成了鲍曼不动杆菌中的 α-Kdo-(2→5)[α-Kdo-(2→4)]α-Kdo 三糖,最终三糖产物 19 的产率为 70%,去除三糖 19 的硫醚基团后得到三糖 20,产率为 88%。其中,鲍曼不动杆菌 LPS 三糖已被证明可潜在作为用于开发针对鲍曼不动杆菌的诊断工具和疫苗的最小表位。事实上,研究团队将该三糖的合成路线进一步缩短与优化,为三糖的合成及应用提供了新选择。为了进一步扩大上述方法的应用范围,试验最后还尝试了合成 4,5,7,8-支链 Kdo 五糖,在鲍曼不动杆菌 LPS 三糖的基础上,研究团队在核心 Kdo 的 7,8 位各引入了一个 Kdo 分子,最终得到目标五糖 26 的产率为 85%。
(来源:上述论文)确定亚磷酸酯之后,该团队进行了底物范围研究,在糖基亚磷酸酯供体活化条件下,经修饰的 Kdo 亚磷酸酯糖基供体 1 可以在 5 分钟内完全活化,并产生了 Kdo 糖苷 3a,其产率 为 91%,且未形成 2,3-烯副产物。接下来,经修饰的 α-Kdo 亚磷酸酯供体 1与各种受体 2a- 2r 进行糖基化反应,产生 Kdo 糖苷 3a-3r 的产率约为 79%-97%之间。随后,该团队筛选了⼀系列自由基反应去除对甲苯硫基,选定条件下,大部分对甲苯硫基被有效去除,且生产 α-Kdo 糖苷产物 4a‒4o 的产率在 79%‒96%。然后,将供体 1 与一级和次级糖基受体 5a-5l 偶联产生 α-Kdo 二糖 6a–6l,产率约在 85%–98% 区间。为了证明亚磷酸酯供体 1 和硫代糖苷的正交性,研究团队合成了硫代葡萄糖苷受体 5j‒5l 并分别与供体 1 偶联,结果显示所合成的 α-Kdo 的二糖 6j、6k 以及 6l,产率分别是 90%、90% 和 85%。为了验证上述方法在生成 Kdo 天然低聚糖中的实用性,研究团队尝试合成 Kdo-α-(2→6)-GlcN-β-(1→6)-GlcN 三糖。在试验中,他们以供体 12 和 6-OH 受体在 5 天内合成葡萄糖胺二糖 13,优化条件后,最终得到三糖 15 的产量率为 93%。去除对甲苯硫基后,三糖 16 的产率为 82%。通过一系列试验,研究人员证明了亚磷酸酯供体和硫代糖苷供体的正交性,这为构建 Kdo 复合寡糖提供了新的选择。后续,研究团队还合成了鲍曼不动杆菌中的 α-Kdo-(2→5)[α-Kdo-(2→4)]α-Kdo 三糖,最终三糖产物 19 的产率为 70%,去除三糖 19 的硫醚基团后得到三糖 20,产率为 88%。其中,鲍曼不动杆菌 LPS 三糖已被证明可潜在作为用于开发针对鲍曼不动杆菌的诊断工具和疫苗的最小表位。事实上,研究团队将该三糖的合成路线进一步缩短与优化,为三糖的合成及应用提供了新选择。为了进一步扩大上述方法的应用范围,试验最后还尝试了合成 4,5,7,8-支链 Kdo 五糖,在鲍曼不动杆菌 LPS 三糖的基础上,研究团队在核心 Kdo 的 7,8 位各引入了一个 Kdo 分子,最终得到目标五糖 26 的产率为 85%。 ▲图 | 合成五糖(来源:上述论文)“与大多数直接糖基化方法相比,这种新方法保护基选择更容易,反应体系更清洁,产物更容易分离。未来,我们将通过这种方法合成更多的 Kdo 寡糖,而且会持续从生物学角度评价合成的 Kdo 寡糖。”参考资料:1.https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.202313985素材来源官方媒体/网络新闻免责声明:本文旨在传递合成生物学最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。欢迎合成生物学领域科研从业者扫码加群,加好友请备注“单位+领域+职位”(不加备注不予通过)↓↓↓
▲图 | 合成五糖(来源:上述论文)“与大多数直接糖基化方法相比,这种新方法保护基选择更容易,反应体系更清洁,产物更容易分离。未来,我们将通过这种方法合成更多的 Kdo 寡糖,而且会持续从生物学角度评价合成的 Kdo 寡糖。”参考资料:1.https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.202313985素材来源官方媒体/网络新闻免责声明:本文旨在传递合成生物学最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。欢迎合成生物学领域科研从业者扫码加群,加好友请备注“单位+领域+职位”(不加备注不予通过)↓↓↓


合肥科生景肽生物科技有限公司成立于2018年,目前已经打造了全球领先的以肽为核心的生命分子发现、合成生产、结构优化、递送平台,主要瞄准肽发现及靶向递送,专注于为各大制药企业、生物技术公司、科研单位提供一站式的定制化研发服务。
公司独有的KPDS™平台(KS-V Peptide Discovery Services Platform)是国际领先的的多肽药物发现平台,我们致力于创新药物的高效和精准开发,以科生景肽专有KPDS技术为核心,提供一站式,定制化的多肽发现服务,以灵活的产品形式和服务模式助力广大客户各类药物发现项目的快速推进和应用探究,包括但并不限于疾病诊断及保健功能产品、多肽药物、核素偶联药物(RDC)、基于小分子的肽药物偶联物(PDC)和多功能肽偶联物等。
 3-去氧-D-甘露-辛酮糖酸(Kdo)是一种单糖,这是细菌表面多糖的重要组成部分,广泛存在于细菌的脂多糖及荚膜多糖中。其对维持细菌细胞壁以及外膜的完整性具有重要作用。如果能实现 Kdo 糖苷的高效率、高选择性合成,将为抗菌疫苗及新型抗生素的开发带来更多新的选择。然而,目前 Kdo 糖基化面临着难以控制选择性、反应活性低等诸多难题和挑战。不久前,北京大学药学院的研究人员报道了一种高效简洁的糖基化方法,这是一种合成 α-Kdo (α-3-Deoxy-d-manno-oct-2-ulosonic Acid)糖苷的间接方法,即通过 3 位硫醚取代 Kdo 糖基供体高效合成一系列 α-Kdo 糖苷,产率最高达 98%。然后,通过分步或一锅法合成了多种天然低聚糖,包括 Kdo 五糖。这项研究已经发表在了 Angewandte Chemie International Edition 上。
3-去氧-D-甘露-辛酮糖酸(Kdo)是一种单糖,这是细菌表面多糖的重要组成部分,广泛存在于细菌的脂多糖及荚膜多糖中。其对维持细菌细胞壁以及外膜的完整性具有重要作用。如果能实现 Kdo 糖苷的高效率、高选择性合成,将为抗菌疫苗及新型抗生素的开发带来更多新的选择。然而,目前 Kdo 糖基化面临着难以控制选择性、反应活性低等诸多难题和挑战。不久前,北京大学药学院的研究人员报道了一种高效简洁的糖基化方法,这是一种合成 α-Kdo (α-3-Deoxy-d-manno-oct-2-ulosonic Acid)糖苷的间接方法,即通过 3 位硫醚取代 Kdo 糖基供体高效合成一系列 α-Kdo 糖苷,产率最高达 98%。然后,通过分步或一锅法合成了多种天然低聚糖,包括 Kdo 五糖。这项研究已经发表在了 Angewandte Chemie International Edition 上。 (来源:Angewandte Chemie International Edition)本研究的通讯作者是北京大学药学院化学生物学系主任、教授李中军和助理研究员李忠堂。李中军的重点研究方向是探索寡糖合成方法学及快速组装策略、糖为手性源的天然产物和合成与活性、 基于糖的化学生物学研究以及创新药物研发。Kdo 糖基化是合成多种 α-Kdo 糖苷的重要方法,然而这是最具挑战性的糖基化反应之一。也因此,领域内一直在探索开发出高效且具有立体选择性的糖基化方法。现阶段,领域内已经开发出了多种方法,包括直接法和间接法。前者需要选择合适的保护基,且糖基化过程会产生 2,3-烯(2,3-ene)副产物;间接法通常需要添加一个或多个步骤构建具有完全立体调节性的目标糖苷,与直接方法相比,这种方法极大简化了保护基的选择,提高了效率和立体选择性。不过,间接法存在增加了反应步骤,且不易选择合适的辅助基团等问题。在这项研究中,该团队开发出了一种更高效、便捷实现 Kdo 糖基化的间接方法。他们通过轴向键在 Kdo 的 C3 位置上引入对甲苯硫基(p-tolylthio group),基于经修饰的 Kdo 亚磷酸酯供体合成了多种 α-Kdo 糖苷和几种极具挑战性的 Kdo 寡糖。值得一提的是,这一过程中并没有形成 2,3-烯副产物,对甲苯硫基也可以通过自由基还原轻松清除。
(来源:Angewandte Chemie International Edition)本研究的通讯作者是北京大学药学院化学生物学系主任、教授李中军和助理研究员李忠堂。李中军的重点研究方向是探索寡糖合成方法学及快速组装策略、糖为手性源的天然产物和合成与活性、 基于糖的化学生物学研究以及创新药物研发。Kdo 糖基化是合成多种 α-Kdo 糖苷的重要方法,然而这是最具挑战性的糖基化反应之一。也因此,领域内一直在探索开发出高效且具有立体选择性的糖基化方法。现阶段,领域内已经开发出了多种方法,包括直接法和间接法。前者需要选择合适的保护基,且糖基化过程会产生 2,3-烯(2,3-ene)副产物;间接法通常需要添加一个或多个步骤构建具有完全立体调节性的目标糖苷,与直接方法相比,这种方法极大简化了保护基的选择,提高了效率和立体选择性。不过,间接法存在增加了反应步骤,且不易选择合适的辅助基团等问题。在这项研究中,该团队开发出了一种更高效、便捷实现 Kdo 糖基化的间接方法。他们通过轴向键在 Kdo 的 C3 位置上引入对甲苯硫基(p-tolylthio group),基于经修饰的 Kdo 亚磷酸酯供体合成了多种 α-Kdo 糖苷和几种极具挑战性的 Kdo 寡糖。值得一提的是,这一过程中并没有形成 2,3-烯副产物,对甲苯硫基也可以通过自由基还原轻松清除。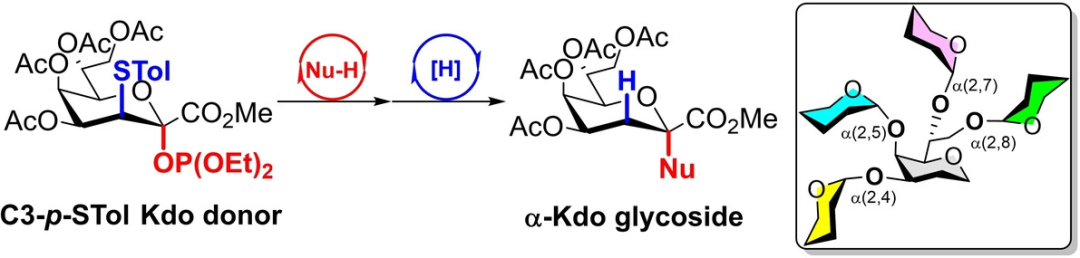 (来源:上述论文)确定亚磷酸酯之后,该团队进行了底物范围研究,在糖基亚磷酸酯供体活化条件下,经修饰的 Kdo 亚磷酸酯糖基供体 1 可以在 5 分钟内完全活化,并产生了 Kdo 糖苷 3a,其产率 为 91%,且未形成 2,3-烯副产物。接下来,经修饰的 α-Kdo 亚磷酸酯供体 1与各种受体 2a- 2r 进行糖基化反应,产生 Kdo 糖苷 3a-3r 的产率约为 79%-97%之间。随后,该团队筛选了⼀系列自由基反应去除对甲苯硫基,选定条件下,大部分对甲苯硫基被有效去除,且生产 α-Kdo 糖苷产物 4a‒4o 的产率在 79%‒96%。然后,将供体 1 与一级和次级糖基受体 5a-5l 偶联产生 α-Kdo 二糖 6a–6l,产率约在 85%–98% 区间。为了证明亚磷酸酯供体 1 和硫代糖苷的正交性,研究团队合成了硫代葡萄糖苷受体 5j‒5l 并分别与供体 1 偶联,结果显示所合成的 α-Kdo 的二糖 6j、6k 以及 6l,产率分别是 90%、90% 和 85%。为了验证上述方法在生成 Kdo 天然低聚糖中的实用性,研究团队尝试合成 Kdo-α-(2→6)-GlcN-β-(1→6)-GlcN 三糖。在试验中,他们以供体 12 和 6-OH 受体在 5 天内合成葡萄糖胺二糖 13,优化条件后,最终得到三糖 15 的产量率为 93%。去除对甲苯硫基后,三糖 16 的产率为 82%。通过一系列试验,研究人员证明了亚磷酸酯供体和硫代糖苷供体的正交性,这为构建 Kdo 复合寡糖提供了新的选择。后续,研究团队还合成了鲍曼不动杆菌中的 α-Kdo-(2→5)[α-Kdo-(2→4)]α-Kdo 三糖,最终三糖产物 19 的产率为 70%,去除三糖 19 的硫醚基团后得到三糖 20,产率为 88%。其中,鲍曼不动杆菌 LPS 三糖已被证明可潜在作为用于开发针对鲍曼不动杆菌的诊断工具和疫苗的最小表位。事实上,研究团队将该三糖的合成路线进一步缩短与优化,为三糖的合成及应用提供了新选择。为了进一步扩大上述方法的应用范围,试验最后还尝试了合成 4,5,7,8-支链 Kdo 五糖,在鲍曼不动杆菌 LPS 三糖的基础上,研究团队在核心 Kdo 的 7,8 位各引入了一个 Kdo 分子,最终得到目标五糖 26 的产率为 85%。
(来源:上述论文)确定亚磷酸酯之后,该团队进行了底物范围研究,在糖基亚磷酸酯供体活化条件下,经修饰的 Kdo 亚磷酸酯糖基供体 1 可以在 5 分钟内完全活化,并产生了 Kdo 糖苷 3a,其产率 为 91%,且未形成 2,3-烯副产物。接下来,经修饰的 α-Kdo 亚磷酸酯供体 1与各种受体 2a- 2r 进行糖基化反应,产生 Kdo 糖苷 3a-3r 的产率约为 79%-97%之间。随后,该团队筛选了⼀系列自由基反应去除对甲苯硫基,选定条件下,大部分对甲苯硫基被有效去除,且生产 α-Kdo 糖苷产物 4a‒4o 的产率在 79%‒96%。然后,将供体 1 与一级和次级糖基受体 5a-5l 偶联产生 α-Kdo 二糖 6a–6l,产率约在 85%–98% 区间。为了证明亚磷酸酯供体 1 和硫代糖苷的正交性,研究团队合成了硫代葡萄糖苷受体 5j‒5l 并分别与供体 1 偶联,结果显示所合成的 α-Kdo 的二糖 6j、6k 以及 6l,产率分别是 90%、90% 和 85%。为了验证上述方法在生成 Kdo 天然低聚糖中的实用性,研究团队尝试合成 Kdo-α-(2→6)-GlcN-β-(1→6)-GlcN 三糖。在试验中,他们以供体 12 和 6-OH 受体在 5 天内合成葡萄糖胺二糖 13,优化条件后,最终得到三糖 15 的产量率为 93%。去除对甲苯硫基后,三糖 16 的产率为 82%。通过一系列试验,研究人员证明了亚磷酸酯供体和硫代糖苷供体的正交性,这为构建 Kdo 复合寡糖提供了新的选择。后续,研究团队还合成了鲍曼不动杆菌中的 α-Kdo-(2→5)[α-Kdo-(2→4)]α-Kdo 三糖,最终三糖产物 19 的产率为 70%,去除三糖 19 的硫醚基团后得到三糖 20,产率为 88%。其中,鲍曼不动杆菌 LPS 三糖已被证明可潜在作为用于开发针对鲍曼不动杆菌的诊断工具和疫苗的最小表位。事实上,研究团队将该三糖的合成路线进一步缩短与优化,为三糖的合成及应用提供了新选择。为了进一步扩大上述方法的应用范围,试验最后还尝试了合成 4,5,7,8-支链 Kdo 五糖,在鲍曼不动杆菌 LPS 三糖的基础上,研究团队在核心 Kdo 的 7,8 位各引入了一个 Kdo 分子,最终得到目标五糖 26 的产率为 85%。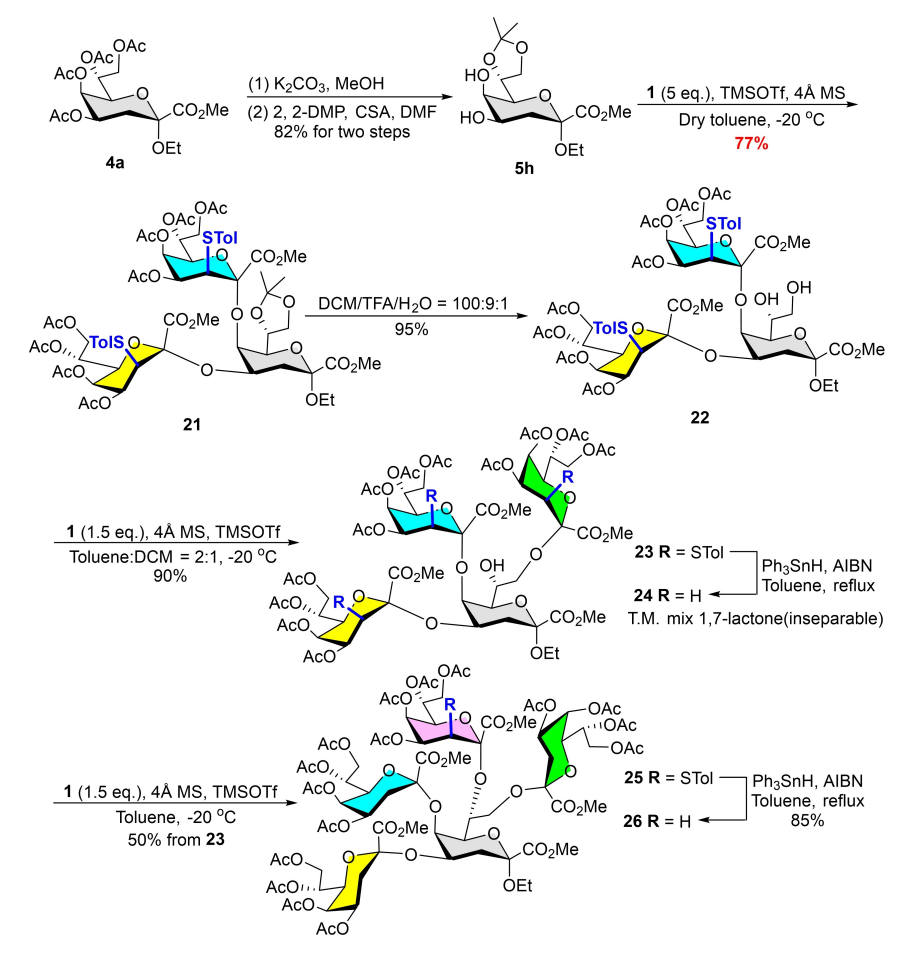 ▲图 | 合成五糖(来源:上述论文)“与大多数直接糖基化方法相比,这种新方法保护基选择更容易,反应体系更清洁,产物更容易分离。未来,我们将通过这种方法合成更多的 Kdo 寡糖,而且会持续从生物学角度评价合成的 Kdo 寡糖。”参考资料:1.https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.202313985素材来源官方媒体/网络新闻免责声明:本文旨在传递合成生物学最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。欢迎合成生物学领域科研从业者扫码加群,加好友请备注“单位+领域+职位”(不加备注不予通过)↓↓↓
▲图 | 合成五糖(来源:上述论文)“与大多数直接糖基化方法相比,这种新方法保护基选择更容易,反应体系更清洁,产物更容易分离。未来,我们将通过这种方法合成更多的 Kdo 寡糖,而且会持续从生物学角度评价合成的 Kdo 寡糖。”参考资料:1.https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.202313985素材来源官方媒体/网络新闻免责声明:本文旨在传递合成生物学最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。欢迎合成生物学领域科研从业者扫码加群,加好友请备注“单位+领域+职位”(不加备注不予通过)↓↓↓


中文官网地址:https://www.ks-vpeptide.com.cn/
英文官网地址:https://www.ks-vpeptide.com
领英:https://www.linkedin.com/company/ks-v-peptide/
© 版权声明
THE END