摘要:介绍了多肽固相合成反应原料———保护氨基酸的制备、应用进展, 详细讨论了氨基酸的α-氨基、α-羟基以及侧链活性基团的各种新型保护基团, 概括了新型保护氨基酸的结构特点和应用条件, 并对保护氨基酸今后的发展方向进行了展望。
关键词: 固相多肽合成氨基酸 保护
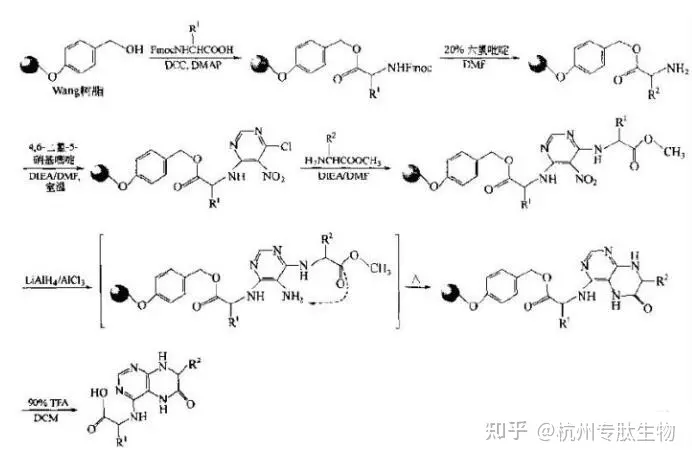
1962年, Merrifield创立了固相多肽合成法 [1] , 自此以保护氨基酸为原料的固相合成以其特有的优势引起了人们的注意。在此后的几10年间, 多肽同相合成不断完善, 从小规模、短肽链合成发展到大规模、长肽链的合成。2003年上市的抗爱滋病药物T—20就是一个全合成的36个氨基酸残基组成的小肽药物。上世纪90年代, 组合化学与多肽合成技术相结合后, 又出现了组合肽库的合成, 对化学、生化、医药、分子生物学等领域起到了巨大的推动作用。在发展过程, 对保护氨基酸的要求也不断提高, 使之不断改进。
固相多肽合成中要求参与反应的原料氨基酸不参与形成肽键的活泼官能团受到保护, 同时反应结束后, 可以将这些活性基团的保护基切除。
在选择氨基酸保护基团时, 要充分考虑反应选择性的问题, 即α-氨基保护基团和α-羧基保护基团是暂时性保护基团, 一个氨基酸结合到肽链上后, 要能立刻脱除;而侧链保护基团是“永久性”保护基团, 在肽的合成过程中不会受到反应物的影响, 不发生反应, 当肽合成结束后再最后脱除。所以侧链保护基团的稳定性要大于α-氨基保护基团和α-羧基保护基团。
保护氨基酸的选择直接关系到合成产物的得率与纯度, 反应中形成的副产物和消旋化为纯化带来很大的困难, 因而开发新型的保护氨基酸是固相多肽合成的重要组成部分。
目前氨基酸保护主要分为3类:α-氨基保护、α-羧基保护以及侧链活性基团保护。本文以这3个分类为基础, 重点介绍了近年来保护氨基酸的一些新品种及其结构特点和应用条件。
1 α-氨基保护
氨基原则上可采用酰化、烷基化、烷基酰化等反应进行可逆屏蔽。基于硫和磷衍生物的保护基团也有报道。过去10年, 发展了上百种不同的氨基保护基团, 主要包括烷氧羰基型保护基团、酰基型保护基团和烷基型保护基团。已报道的研究结果表明, 不存在一种通用的理想氨基保护基团用于多肽固相合成。
1.1 烷氧羰基型 (氨基甲酸酯型) 保护基团
这类保护基团与氨基酸结合后的形式为:

其中

:苄氧羰基 (Z) ;b:叔丁氧羰基 (Boc) ;c:9-芴氧羰基 (Fmoc) ;d:2- (4-硝基苯磺酰基) 乙氧羰基 (Nsc) ;e:1, 1-二氧苯基 (邻) 2-噻吩甲氧羰基 (Bsmoc) ;f:2- (甲磺酰基) -3-苯基-2-丙烯氧羰基 (Mspoc) ;g:2- (叔丁磺酰基) -2-丙烯氧羰基 (Bspoc) :h:环戊烷氧羰基 (Poc)
Z、Boc、Fmoc是最常见的3种氨基保护基团。Z是一种使用时间很长的氨基保护基, 至今仍有广泛应用。其优点是制备容易:得到的Z-氨基酸易结晶并且稳定;活化时不易消旋;可以在H2/Pd、HBr/AcOH、Na/液氨等条件下脱去该保护基团 [2] 。Boc可用于大部分多肽合成的偶联过程, 可以在酸解条件下除去, 同时可避免受到催化氢化、碱水解和钠/液氨还原的影响。Boc通常在无水TFA、0℃反应条件脱除 [2] 。Fmoc是氨基甲酸酯型氨基酸保护基团中, 唯一广泛应用的可以在弱碱条件下解离的基团, Fmoc脱保护可使用稀哌啶溶液或二乙胺DMF溶液, 在室温下完成 [3] 。
随着对氨基保护认识的不断深入, 在上述3种保护基团的基础上进行官能团修饰, 得到了一些选择性或稳定性更好的氨基保护基团。
Nsc被认为是一种比Fmoc更好的保护基团。Nsc在碱性条件下更加稳定, 对弱碱性溶剂更不敏感。Nsc比Fmoc亲水性更强, 形成天冬酰胺的可能性进一步减小 [4] 。与Fmoc一致的是, Nsc在脱保护反应中形成石蜡, 最终与哌啶加合反应。但在Fmoc反应中, 二苯基富烯哌啶加合物的形成是可逆的, 而Nsc反应形成的加合物是不可逆的, 这样可减少发生副反应的几率 [5] 。Nsc可在室温下用哌啶、2-氨基乙醇、吗啉、液氨等脱除。
Carpino 等人发展了一系列新型碱不稳定氨基保护基团Bsmoc、Mspoc和Bspoct [6~8] 。这类基团解离需要加入亲核试剂 (如仲胺) , 伴随释放氨基甲酸酯。Bsmoc对酸和叔胺稳定, 但当仲胺存在时很容易发生解离反应。由于脱保护过程同时也是消除反应, 所以很少发生副反应。
Poc是一种不同于Boc和Fmoc的氨基保护基团, 它既对酸稳定, 同时对碱也稳定, Surajit等人发现25℃与三氟乙酸反应1 h, Poc基团仍然很稳定, 而叔丁基等侧链保护基团则能够完全脱除, 利用这一特点可以选择性的脱除侧链保护基 [9] 。Poc基团可在超声波搅动下, 用四硫钼酸盐脱去, 还可用HBr/AcOH或Na/液氨脱除。
1.2 酰基型保护基团
这类保护基团主要有羧酰基型和苯磺酰基型两类, 与氨基酸结合后形式如下:

a:三氟乙酰基 (Tfa) ;b:对甲苯磺酰基 (Tos) ;c:邻位硝基苯磺酰基 (oNbs)
Tfa最早由Weygand在1952年引入多肽合成 [2] , 其脱除条件相对温和, 用哌啶或氢氧化钠处理可容易地脱去。但活化时容易消旋, 并且在碱水解时容易断链, 所以被广泛应用。
Tos也是早期使用的保护基团 [3] , 稳定性非常好,只能用Na/液氨处理脱去, 不受酸碱作用或催化氢解作用影响。但由于Na/液氨处理操作麻烦, 并且会导致某些肽键的断裂, 因此目前较少使用。
在Tos的苯环上引入邻位硝基, 得到oNbs后, 情况就得到很大的改善 [10] 。磺胺保护基团允许氨基酸的N-酰化, 而没有吡酮作用机理产生的消旋化。并且此保护基团用苯硫酚或烷烃硫醇处理就可除去, 克服了Tfa和Tos不易脱除的缺点。
1.3 烷基型保护基团

a:三苯甲基 (Trt) ;b:N-1- (4, 4-二甲基-2, 6-二氧环亚己基) 乙基 (Dde) ;c:N-1- (4-硝基-1, 3-二氧茚满-2-烯) 乙基 (Nde)
Trt是很常用的烷基型保护基团 [2] , 脱除的条件温和, 可以用无水HCI/MeOH、TFA或HBr/AcOH脱去。由于Trt有很大的立体空间位阻, 一般很难导入与氨基结合, 并且侧链上的Trt比主链上的Trt稳定, 因此Trt的应用多用于侧链氨基酸的保护, 而对α-氨基的保护应用较少。
Dde和Nde是新型的烷基型氨基保护基团。Dde对TFA和哌啶很稳定, 要用2% (v/v) 的肼/DMF脱去, 因此选择合适的脱保护条件, 就可以保留主链上的氨基保护, 而脱去侧链上的氨基保护基团, 进而合成支链肽。
Barrie Kellam等人研究了Dde的特点, 在此基础上, 得到的Nde显示了良好的酸、二级/三级碱稳定性 [11] 。与Dde类似, Nde的结构不能形成唑酮, 有效的降低了消旋化, 可用2% (v/v) 的肼/DMF脱保护除去。其中茚满基团的加入可以既增强亲核进攻, 又可以提高UV吸收值, 利于在线检测。
2 α-羧基保护
多肽固相合成—般不需要进行α-羧基的保护, 只有在极少数条件下, 有必要保护α-羧基。如合成谷胱甘肽, 要求谷氨酸的γ-羧基进行反应, 而α-羧基则需要保护。目前羟基保护基团大致分为两类:酯基、酰肼。
2.1 酯基
采用酯基保护羟基是最常用的方法, 主要有以下几种类型:

a:甲酯 (Me) ;b:乙酯 (Et) ;c:叔丁酯 (tBu) ;d:苄酯 (Bzl) ;e:2, 4-二甲基氧苯甲基酯 (2, 4-Dmb)
其中Me、Et和Bzl制备方法简单, 可以用碱皂化脱去。tBu是目前最常用的羧基保护基团之一。tBu相对于Me和Et更稳定, 不易被碱皂化脱, 但能用HCI、HBr/AcOH、TFA、HF等酸解脱去。酸敏性酯2, 4-Dmb用1%TFA/CH2Cl2处理即可脱除, 而不会引起其它侧链保护脱除, 这种选择性可以在一些特殊情况下使用, 如侧链羟基与主链氨基结合制备环肽 [12] 。
2.2 酰肼
酰肼也用于Cα或侧链羧基的保护, 但是在这种情况下, 必须进一步叠氮偶联, 在固相多肽合成中应用较少。其形式一般为:NH2CHRCONHNHR’。
3侧链活性基团保护
3.1 ω-羧基保护基团
天冬氨酸 (Asp) 和谷氨酸 (G1u) 具有两个羧基, 在碱或者强酸的作用下, 侧链上ω-羧基容易发生副反应。如天冬氨酸在活化时形成的侧链酯经相应的琥珀酰亚胺中间态生成异天冬酰胺肽。常用的保护基团有在Fmoc策略中使用的叔丁基酯基 (OtBu) 和在Boc策略中使用的β-环己基酯基 (OcHex) 。这两种保护基团通常可以抑制上述副反应的发生, 但是当Asp与Gly、Thr (tBu) 、Cys (Acm) 连接时, 副反应十分剧烈, 必须采用N-2-羟基-4-甲氧基苯基 (Hmb) 保护 [13] 。脱去保护基时, 可用TFA处理, 加入硫醇捕捉碳正离子, 减少副反应发生。
Karlstr⌀m和Undén合成了β-2, 4-二甲基-3-戊酯基 (ODmp) 和β-3-甲基戊—3-酯基 (OMpe) 两种保护基团 [14] 、 [15] 。实验发现ODmp和OMpe可非常有效的抑制天冬氨酸的天冬酰胺转化晌副反应, 比OtBu、OcHex更能阻止天冬酰亚胺的形成, 可用于困难片断的合成。

3.2 羟基保护
酪氨酸 (Tyr) 的酚羟基、丝氨酸 (Ser) 和苏氨酸 (Thr) 的羟基都是活泼基团, 必须在多肽固相合成过程中加以保护。常用基团有在Boc策略中使用的2-溴苯氧羰基 (BrZ) 、苄基 (Bzl) , 以及在Fmoc策略中使用的叔丁基 (tBu) 。BrZ主要保护Tyr的酚羟基, 对亲核试剂和TFA十分稳定, 需要用强酸脱除;对碱极不稳定, 20%哌啶中完全解离。Bzl可用氢解、HF、Na/液氨脱除, 在TFA中会有部分解离。tBu可用TFA (室温下反应2 h) 、HCI/TFA或用浓HCl 10℃反应10 min脱去。
Rosenthal等人采用2, 4-二甲基戊氧羰基 (Doc) 作为Tyr的保护基团, 在Boc策略下保护效果较好。Doc对哌啶的稳定性是BrZ的1 000倍, 同时可用HF完全脱除 [16] 。
Nishiyama等合成的环己基酯基 (cHex) 是一种较合适的保护基团, 与Bzl相比, cHex在50%的TFA/DCM中更加稳定, 并且不会形成重排副产物, 同时对20%哌啶也稳定, 因此不但可用于Boc策略, 同时可以用于Fmoc策略, 但是合成比较困难 [17] 。
在研究上述所有基团的基础上, József Bódi等研究了一种cHex的开环类似物:3-戊烷基 (Pen) 。它不但在50%的TFA/DCM中稳定, 而且在20%的哌啶/DMF中也稳定, 因此既可用于Boc策略, 又可以用于Fmoc策略, 合成也较cHex容易 [18] 。Pen基团的脱除采用HF方法。

3.3 吲哚保护
Fmoc策略中色氨酸 (Trp) 一般不需要侧链保护, 但最后其它侧链氨基酸保护基脱除时, 吲哚的叔丁基化和磺化作用会加剧。采用Boc基团保护是阻止上述副反应的一种好方法。
Boc策略合成含有Trp的多肽时, 吲哚易发生环化或二聚反应, 因此必须保护吲哚部分。通常用Nin—甲酸基 (For) 基团保护, For对反复的TFA的处理稳定, 可用碱或HF/硫醇除去。但是也带来其它问题, 如臭味、硫醇的聚合副反应。此外, Z基团和1, 3, 5-三甲基苯磺酰基 (Mts) 可用于保护Trp。但是Z基团用HF脱保护方法除去时, 反应不完全;而Mts基团在肽合成过程中, 会被TFA逐渐分解。
Yuji Nishiuchi等人总结Z和Mts的特点, 引入了环己基氧羰基 (Hoc) 基团。氨基甲酸酯型Hoc基团的解离, 会形成羧酸酯中间态, 减少Trp吲哚环上的亲核进攻 [19] 。此外Hoc基团上的碳环, 可以增加对碱和酸的稳定性。实验结果表明, Hoc在肽链延长时非常稳定, 能在不使用硫醇的条件下用HF除去。

3.4 巯基保护
半胱氨酸中巯基具有强亲核性、易氧化性和酸性等特性, 要求在所有合成过程中将巯基选择性屏蔽。常用的保护基团有Trt、tBu、乙酰胺甲基 (Acm) , 脱保护条件各不相同。Trt是应用最广的保护基团, 可以用HF、TFA、I2、Hg (Ⅱ) 等脱除;tBu可用TFMSA脱除:Acm可用I2、Hg (Ⅱ) 脱除。在上述基团的基础上进行修饰, 得到类似的叔丁基硫烷基 (StBu) [20] 和三甲基乙酰胺甲基 (Tacm) [21] , 这两种基团的稳定性有所增加, 同时制备方法更简单。利用各保护基团脱保护条件的差别, 可以选择性进行二硫键的形成。
亚磺酰硝基嘧啶 (Npys) 是一种新型巯基保护基团 [22] , 对碱极不稳定, Fmoc策略不能使用。但是若采用Boc策略, 则可以将其保护的半胱氨酸引入N端, 在弱碱性条件下, 就可除去, 从而可以方便的进行环化反应。

3.5 咪唑保护
组氨酸 (His) 是多肽合成中问题最大的氨基酸之一。当组氨酸的咪唑环未被保护时, 主要存在两个问题:N-酰化和消旋化。可逆性的屏蔽眯唑官能团可以避免这些问题。Boc策略中早期采用的保护基团有Boc和Tos。其中Boc基团会与α-氨基保护基团同时脱除, 导致每一步缩合反应都有酰化和消旋化发生, 因此目前应用很少。Tos是Boc策略中最常见的His保护基团。溶解性好, 并且容易脱除, 可以采用HF或TFMSA处理。但Tos基团也有不足, 在HOBt作用下会有部分脱除, 因此采用HOBt/DCC活化时, 会有苯甲磺酰化等副反应发生。
苄氧甲基 (Bom) 基团弥补了上述基团不足 [23] , Bom可以完全屏蔽咪唑基团引起消旋化的π-氮原子, 缩合反应条件下也很稳定, 采用HF或TFMSA处理即可脱去。
Fmoc策略中, 组氨酸眯唑最常用的保护基团是Trt。Trt屏蔽咪唑基团π-氮原子, 可以有效抑制消旋化发生。尽管由于Trt空间位阻较大, 导致反应比较缓慢, 但是Trt的空间位阻可以有效地减少碱催化的重排作用, 减少了副反应的发生。Trt在肽合成过程中十分稳定, 合成后, 用95%TFA可以很容易脱去。
Nπ-烯丙基 (All) 和Nπ-烯丙基氧甲基 (AIom) [24] 是一类新型的保护基团。All、Alom作用于咪唑基团的π-氮原子, 可以抑制消旋化发生;同时对酸和碱都很稳定, 可用于Fmoc和Boc策略, 制备比较容易, 用亲核试剂与钯即可脱除。

3.6 ε-氨基保护
赖氨酸 (Lys) 的ε-氨基碱性很强, 同时具有亲核性。Boc策略中, 通常用2-氯苯甲氧羰基[Z (2-Cl) ]保护, 对酸稳定性较好, 在解离Boc基团过程中, 可以防止提前脱去侧链保护基团的现象发生。Fmoc策略中, Boc基团是比较好的保护基团, 对碱的稳定性好, 可以有效抑制副反应的发生。
前面介绍的Npys、Dde、Tfa等保护基团也可以用于保护Lys, Npys和Tfa对哌啶不稳定, 一般用于Boc策略, Dde须用肼解脱除, 既可用于Fmoc策略, 又可用于Boc策略。
Dde基团也有其局限性, 合成长肽时, 在哌啶的作用下会有部分解离, 同时发生迁移现象。Sefan Matysiak等人合成的单甲氧基三苯甲基 (Mmt) 和二甲氧基三苯甲基 (Dmt) , 对碱的稳定性增强, 可用于Fmoc策略 [25] 。同时Mint和Dmt对酸极不稳定, 可用醋酸/三氟乙醇/二氯乙烷 (1∶2∶7, v/v) 脱去, 而不会影响其它侧链基团, 因此可用于环肽和支链的合成。
3.7 胍基保护
尽管精氨酸胍基具有强碱性, 在正常反应条件下被质子化作用保护, 但是在活化时, 其对应生成的活化酯在有机溶剂中溶解性低, 不利于多肽合成。在一些条件下, 胍基还会部分酰化, 因此有必要进行保护。
4-甲氧基苯磺酰基 (Mbs) 、Mts、Tos、4-甲氧基-2, 3, 6-三甲基苯磺酰基 (Mtr) 、2, 2, 5, 7, 8-五甲基色满-6-磺酰基 (Pmc) 以及2, 2, 4, 6, 7-五甲基二氢苯并呋喃-5-磺酰基 (Pbf) 等基团是固相合成中常用的精氨酸胍基保护基团 [3] 。酸不稳定性递增, 顺序依次是Tos<Mbs<Mtr<Pmc<Pbf, 其中Pbf表现出最佳脱保护动力学。作为暂时性保护基团Mts与Boc有很好的相容性, 与Tos不同, Mts可用三氟甲烷磺酸 (TFMSA) /TFA/苯甲硫醚除去。Mtr常用于Fmoc策略, 但用TFA/苯甲硫醚脱保护时要求较长的时间。Pmc基团的酸不稳定性与Boc基团类似。所以, Boc (如保护Lys) 和Pmc或Pbf (保护Arg) 可优化组合作为侧链保护基团。
3.8 其它
3.8.1酶解保护基团
合成酸不稳定或碱不稳定肽类衍生物和肽类偶联物时, 其氨基酸的保护基团要求在温和甚至中性反应条件下除去。糖肽、磷肽和脂肽以及含硫酸盐的肽类都属于这类敏感化合物。用碱处理这类衍生物常导致Ser和Thr衍生物的β-消除反应或其它不利的副反应, 而用酸处理则在一些情况下导致偶联物的非肽部分的降解。应用酶解保护基团可以解决上述问题。
四苯甲基葡糖氧羰基 (BGloc) 是氨基甲酸酯型的酶解保护基团[26], 它含有O-苯甲基保护后的葡萄糖作为碳水化合物部分, 它连接着氨基甲酸酯氧原子。除去苯甲基后, 由面包酵母中得到的α-葡萄糖苷酶和由杏仁中得到的β-葡萄糖苷酶两者的混合物, 断开葡萄糖苷键, 从而释放氨基甲酸。可用于保护氨基。
GernotH.M.等人研究的苯基酰肼 (PH) 也是一种酶解保护基团[27], 用于羧基的保护, 可以用蘑菇中提取的酪氨酸酶, 先在酶和氧的作用下生成酰基二氮烯, 再经水解反应完全脱去。
3.8.2光解保护基团
光解保护基团是近几年才发展起来的, 1991年, Fodor首次将光解保护基团邻硝基-3, 4-二甲氧基苯甲氧羰基 (NVOC) 引入作为氨基酸保护基团, 但是NVOC光解速度很慢, 2- (2-硝基苯基) 丙氧羰基 (NPPOC) 是一种新型的光解保护基团, Kumar R.Bhushah等人将它用于氨基的保护, 发现在紫外光照射下, 它的解离速度比NVOC要快2倍[28]。
4讨论与展望
保护氨基酸是多肽合成的关键原料, 保护的策略根据合成肽的方法差异而有所不同。
保护氨基酸的发展重点主要集中在:①对新型α-氨基保护基团的开发, Nsc、Dde、Nde等基团具有降低消旋化、提高脱保护效率等特点;②对侧链活性基团保护的开发, 针对不同活性基团, 分别开发了多种稳定性优良、选择性高、减少副反应发生的保护基团。在实际应用中制备的保护氨基酸显示了优异的性能。
随着合成肽的结构日益复杂, 氨基酸的保护基团越来越趋向于选择性、专一性方向发展, 酶解保护基团和光解保护基团以其特有的优势, 将有可能成为今后研究的新热点。
免责声明:本文为行业交流学习,版权归 原作者所有,如有侵权,可联系删除。返回搜狐,查看更多
合肥科生景肽生物科技有限公司成立于2018年,目前已经打造了全球领先的以肽为核心的生命分子发现、合成生产、结构优化、递送平台,主要瞄准肽发现及靶向递送,专注于为各大制药企业、生物技术公司、科研单位提供一站式的定制化研发服务。 公司独有的KPDS™平台(KS-V Peptide Discovery Services Platform)是国际领先的的多肽药物发现平台,我们致力于创新药物的高效和精准开发,以科生景肽专有KPDS技术为核心,提供一站式,定制化的多肽发现服务,以灵活的产品形式和服务模式助力广大客户各类药物发现项目的快速推进和应用探究,包括但并不限于疾病诊断及保健功能产品、多肽药物、核素偶联药物(RDC)、基于小分子的肽药物偶联物(PDC)和多功能肽偶联物等。中文官网地址:https://www.ks-vpeptide.com.cn/
英文官网地址:https://www.ks-vpeptide.com
领英:https://www.linkedin.com/company/ks-v-peptide/