一、脲键的化学特性与功能优势
脲键(Urea bond)是由两个氨基(-NH₂)通过羰基(C=O)连接形成的化学结构,其化学式为 NH₂-C(=O)-NH₂。该结构具有独特的分子特性:碳原子与两个氮原子通过共轭双键形成刚性平面,同时氮原子上的两个氢原子赋予其氢键供体能力。这种刚柔并济的特性使脲键在药物化学领域展现出显著优势。其在有机化学中常见于尿素、甲基脲等化合物中;在药物化学中,脲键常被用作功能片段,通过调节分子理化性质来改善药物的溶解性和生物活性。脲键的核心优势包括:
1、构像可塑性
平面刚性与动态柔性平衡:脲键具有对称平面结构(与肽键的刚性平面类似),但其氮原子上带有两个氢原子,可形成更多氢键,同时允许一定程度的构象柔性。例如,在刘世勇团队开发的含氨基脲多肽嵌段共聚物(HBCPs)中,脲键的平面性维持了分子整体结构的稳定性,而侧链的烷基取代基则赋予其动态响应能力。
螺旋构象的特殊性:脲类化合物通过分子内氢键网络形成独特的螺旋构象,其方向性(P/M型)可通过端基取代基的氢键竞争性调控实现精准设计。例如,五脲折叠分子在固态下呈现2.512/14螺旋参数,其N端引入叔丁氧羰基(Boc)可增强N→C氢键极性,导致CD3CN中2.1:1的P:M螺旋偏好;而C端烯丙氧羰基则通过削弱C→N氢键反向调节比例。这种动态构象特性使其能够模拟天然蛋白的α螺旋(通过匹配氢键间距与残基排列)或β折叠(依赖π-π堆积与NH-π相互作用),为设计靶向蛋白-蛋白相互作用的药物(如激酶抑制剂、抗菌肽模拟物)提供了高仿生平台。
2、氢键网络特性
氢键供体/受体能力:每个脲键包含 一个羰基氧(氢键受体)和两个氨基氢(氢键供体) ,可同时与多个分子或基团形成氢键。例如,在抗菌肽设计中,脲键的NH基团与细菌膜磷脂的磷酸基团形成多重氢键,增强膜破坏能力。
动态氢键调控:脲键的氢键网络具有pH响应性。例如,在pH敏感的氨基脲键中,酸性条件下(如肿瘤微环境)脲键质子化并断裂,触发药物释放;而在生理pH下恢复稳定,延长循环时间。
3、抗酶解稳定性:脲键的化学稳定性高于肽键,动态脲键(受阻脲键、HUB)可降低抗酶解,尤其在抵抗蛋白酶(如DPP-4、胰蛋白酶)降解方面表现突出。例如,含受阻脲键(HUB)的GLP-1类似物索马鲁肽,在体内抗DPP-4酶解能力是天然肽的30倍,在体内半衰期可延长至48小时以上。实验显示,含脲键多肽在pH 4.0-8.0范围内保持稳定,而普通多肽在极端pH或高温下易水解。
4、溶解性与渗透性优化:通过引入不对称芳基或烷基取代基(如N,N-二异丙基苯基脲)打破分子平面性,降低结晶度,显著提高非极性溶剂中的溶解度。也可以形成伪环结构(分子内NH-π相互作用)减少极性表面积,增强血脑屏障穿透能力。
二、含脲键多肽的构建策略
含脲键的多肽是一种通过化学修饰或合成策略在多肽结构中引入脲键(UB)的化合物,这类多肽结合了传统多肽的功能性特性与脲键的独特理化性。含脲键多肽的的合成方法主要包括:
1、主链修饰:将多肽链中的部分肽键通过固相合成或者化学修饰替换为脲键(-CO-NH-换为-NH-CO-NH-),形成“脲键等排体多肽”。例如,使用二苯碳酸酯(DPC)与氨基酸反应生成苯基脲,避免手性中心异构化。
2、侧链引入:在氨基酸侧链中引入脲基团(赖氨酸的ε-氨基与羰基形成脲键),用于增强分子间相互作用。如中国科学技术大学团队开发的HBCPs(含氨基脲多肽嵌段共聚物),通过NPCA前体直接聚合实现高效合成。
3、末端修饰:在多肽的N端或C端连接含脲键的功能分子(药物偶联物、PH响应型药物载体),以调控其靶向性或稳定性。
4、酶法辅助合成:利用基因编码非天然氨基酸(如脲基赖氨酸),通过工程菌表达或酶促反应形成腙、肟或缩氨基脲键。
三、含脲键多肽的核心特性以及临床应用
含脲键多肽是通过在多肽主链或侧链中引入脲键(-NH-C(=O)-NH-)形成的功能性分子。其独特的化学结构赋予其区别于传统多肽的理化性质和生物学功能。结合最新研究进展和药物设计实践,其主要应用方向包括:
1、生物活性与靶向性
分子识别与靶向递送:脲键的NH基团可与靶蛋白的芳香环(如Trp残基)形成NH-π相互作用,增强结合亲和力。例如,RGD多肽经脲键修饰后对整合素αvβ3的亲和力提升5倍。此外基于脲键的动态氢键网络设计PH/酶响应型药物载体,可以实现肿瘤或炎症部位的精准释药。
抗微生物与抗病毒活性:含脲键的抗菌肽(如Magainin类似物)通过破坏细菌膜脂质双层的氢键网络,对耐药菌(MRSA)的抑菌浓度(MIC)降至0.5 μg/mL。类似策略也可用于抑制病毒膜融合(如HIV gp41靶向抑制剂)。
2、智能药物递送系统
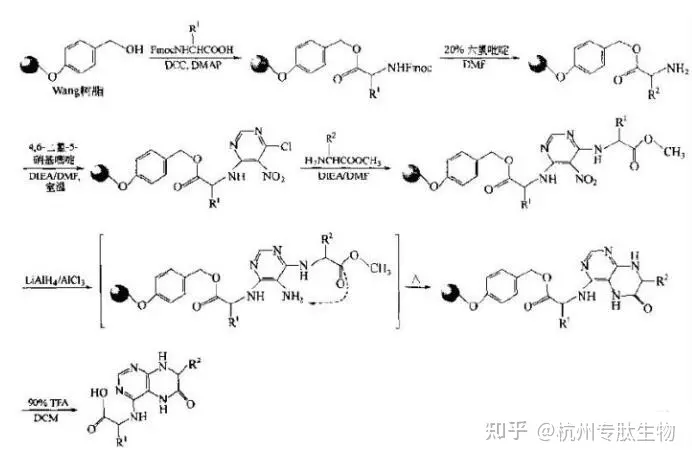
PH响应释放:中国科学技术大学团队(刘世勇、胡进明等,2023)开发了含氨基脲的多肽偶联物(HBCPs),其通过醛/酮衍生物与氨基脲基团的缩合形成pH敏感型缩氨基脲键。该键在肿瘤微环境(pH 6.5-6.8)或溶酶体酸性环境(pH 4.5-5.5)中特异性断裂,释放化疗药物(如阿霉素)。实验表明,该体系能显著提升药物在肿瘤组织的蓄积效率,同时减少全身毒性。
图1 HBCPs合成及应用示意图
溶酶体逃逸增强:氨基脲键的断裂不仅释放药物,还能恢复多肽的氨基脲残基,后者通过质子海绵效应破坏溶酶体膜,促进药物逃逸至细胞质,提高疗效。这种双重功能设计解决了传统多肽药物易被溶酶体降解的难题。
3、功能化与合成优势
化学修饰多样性:脲键可作为多功能连接位点,与醛/酮衍生物形成pH可裂解的氨基脲键,或与金属离子(如Fe³⁺、Cu²⁺)配位构建催化或成像探针。
高效合成策略:使用脲正离子型缩合试剂(如HOBt、HBTU、HATU)实现快速反应、高收率、低消旋的含脲键多肽合成。还可以通过基因编码非天然氨基酸(脲基赖氨酸),利用工程菌直接生产含脲键多肽。
4、应用场景拓展
长效多肽药物:通过脲键替换肽键或引入稳定化侧链,显著延长药物半衰期(如GLP-1类似物、抗菌肽)。将GLP-1类似物(如利拉鲁肽)的肽键替换为脲键,延缓DPP-4酶降解,延长半衰期至24小时以上;设计含脲键的抗菌肽(如Magainin类似物),通过脲基与细菌膜磷脂的磷酸基团形成多重氢键,增强膜破坏作用。
分子影像:含脲键多肽偶联物可通过荧光标记(Cy5.5偶联物)或放射性同位素修饰,实现肿瘤转移灶的高灵敏度成像(检测限达0.5 cm以下)。脲键的化学稳定使其可适用于多种标记技术(近红外荧光、MRI造影剂偶联)且不影响多肽的靶向性。如:聚脲框架材料(如氢键有机框架HOFs)还可负载造影剂,用于深组织成像。
超分子材料:脲键驱动的自组装多肽可形成纳米纤维或水凝胶,用于组织工程支架或药物控释系统。例如:天津医科大学团队设计的自组装六肽负载米托蒽醌和二甲双胍,通过下调PD-L1表达并促进CD8⁺T细胞浸润,显著抑制肿瘤生长,为癌症免疫治疗提供新策略。
四、含脲键多肽与普通肽相比临床应用差异
特性
含脲键多肽
普通多肽多肽
稳定性
抗酶解能力强,热力学稳定性高
易被蛋白酶水解,半衰期短
给药方式
部分可实现口服(磺酰脲类药物)
多需注射
靶向性
通过氢键网络增强与受体结合,提高选择性
依赖天然构像,易受体内环境影响
功能扩展性
可整合成像探针(PH/缺氧响应系统)
功能单一,难以实现诊疗一体化
五、西安纳微生物公司含脲键多肽合成服务
西安纳微生物科技有限公司可为客户提供涵盖含脲键多肽(urea-containing peptides)的设计、合成与应用的全方位服务。
合成能力:支持 5-200 个氨基酸长度,涵盖环肽、线性修饰肽及复杂修饰(荧光标记 / 磷酸化等),规模从毫克级到公斤级。
质控标准:采用 HPLC、质谱及圆二色谱检测,纯度 70%-99%(定制≥98%)。
技术优势:HOAt 缩合试剂、混合溶剂体系及微波辅助合成解决缩合副反应和困难序列问题,结合反相 HPLC 纯化提升产率。
六、总结与展望
含脲键多肽通过氢键动态调控、构象可塑性、抗酶解性三大特性,突破了传统多肽的局限性。其应用已从基础药物设计拓展至靶向治疗、智能材料、分子诊断等前沿领域。未来,结合AI辅助设计(如AlphaFold2预测构象)和合成生物学技术,含脲键多肽有望成为个性化医疗和精准递送系统的核心载体。
【相关文献】
1、Non-isocyanate urethane linkage formation using l-lysine residues as amine sources;
2、《Advanced Materials》,Engineering Semicarbazide-Bearing Polypeptide Co
njugates for Efficient Tumor Chemotherapy and Imaging of Tumor Metastasis;
3、Ajit DhananjayJagtap, Nagendra Bharatrao Kondekar, et al. Ureas: Applications in Drug Design. Curr. Med. Chem. 2017, 24, 622-651;
4、Journal of Medicinal Chemistry, Urea Derivatives in Modern Drug Discovery and Medicinal Chemistry. J.Med. Chem. 2020, 63, 6, 2751–2788;
5、Chem. Soc. Rev., 2023, 52, 2480–2496,Screw sense and screw sensibility: communicating information by conformational switching in helical oligomers,DOI: 10.1039/d2cs00982
6、吴桐1,尹彩云1,赵明哲2,朱颐申1.功能性多肽纳米材料在生物医学诊断领域的应用[J].中国组织工程研究,2023,(第3期).
7、Advanced Science,Intrinsic PD-L1 Degradation Induced by a Novel Self-Assembling Hexapeptide for Enhanced Cancer Immunotherapy
免责声明:文中关于穿膜肽肽的信息是依据现有研究成果和资料整理的,因生物医学研究发展快,这些信息可能存在时效和局限问题。文中案例和成果仅供学术交流参考,不能当作医疗建议、诊断或治疗方案。若有人依据本文信息行事而产生损失、风险或法律责任,作者和发布平台不承担责任,建议寻求专业医学机构和人士获取准确信息与医疗服务。
中文官网地址:https://www.ks-vpeptide.com.cn/
英文官网地址:https://www.ks-vpeptide.com
领英:https://www.linkedin.com/company/ks-v-peptide/